Objectifs du TP
Vous avez à votre disposition différents colorants alimentaires ou des mélanges de ces colorants.
Vous devez réaliser une chromatographie sur couche mince (CCM) de ces colorants afin de déterminer les colorants purs et également identifier la nature des colorants présents dans les mélanges.
Vous rédiger un compte-rendu de TP en binôme.
.
Principe d'une chromatographie sur couche mince
Une CCM, c'est quoi ?
Il s'agit d'une technique d'analyse qui s'appuie sur les différences d'affinités de substances chimiques entre une phase fixe, la plaque, et une phase mobile, l'éluant. Cette différence va permettre la séparation de ces différentes substances sur la plaque.
Utiliser la fiche méthode proposée page 335 ou l'aide en vidéo (Qr-code ci-contre).

Comment identifier les espèces chimiques ?
Chaque espèce chimique s'élève à une hauteur spécifique, c'est ce qui permet de l'identifier par comparaison avec l'élévation d'une espèce témoin.
.
Matériel à votre disposition :
Une cuve à chromatographie (bocal avec son couvercle) | des micro-pipettes |
Un flacon contenant l'éluant | 4 colorants alimentaires dans des tubes à essais |
Une bande de papier Whatman d'environ 5 cm sur 8 cm ; | Un sèche-cheveux. |
.
.
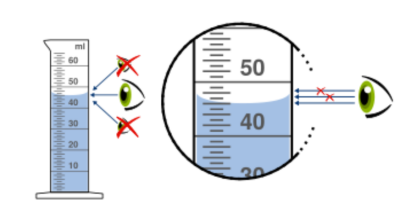
Méthode : de la verrerie adaptée pour mesurer un volume de solution
Vous devez mesurer la masse des éléments de verrerie suivants (ligne 2 du tableau ci-dessous) avec la balance électronique mise à votre disposition.
Mesurer avec chaque élément de verrerie précédent 10,0 mL d'eau distillée en utilisant une petite pipette pour ajuster le niveau si nécessaire puis mesurer la masse correspondante de l'ensemble (eau + élément de verrerie). Indiquer la valeur obtenue dans la ligne 3 du tableau.
3. Déterminer la masse des 10,0 mL d'eau qui ont été mesuré avec chaque élément de verrerie (ligne 4 du tableau).
4. Quelle devrait-être la masse théorique de 10,0 mL d'eau distillée ? Justifier votre réponse.
5. Que pouvez-vous conclure de vos mesures précédentes ?
verrerie utilisée | éprouvette de 10 mL | éprouvette de 25 mL | éprouvette de 100 mL | bécher de .... mL | bécher de 100 mL | fiole jaugée de 10 mL |
masse de l'élément de verrerie seul (en g) | ||||||
masse de l'élément de verrerie et de 10,0 mL d'eau (en g) | ||||||
masse de 10,0 mL d'eau (en g) |
.
Exemple : analyse de médicaments par chromatographie
Utiliser la simulation numérique proposée pour déterminer les constituants des médicaments (Qr-code ci-contre).
Indiquer la constitution de ces gélules et médicaments par écrit.