Polarité d'une molécule
La polarité d'une molécule dépend de la géométrie de la molécule et de l'existence de liaisons polarisées entre deux atomes.
Les atomes d'oxygène et de d'azote ont tendance à former des liaisons polarisées ce qui n'est pas le cas des atomes d'hydrogène et de carbone.
Les molécules qui ne sont pas polaires sont dîtes « apolaires ».
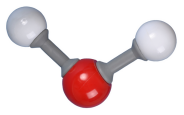 |
En déduire ce qui peut expliquer le caractère polaire de la molécule d'eau alors que la molécule de dioxyde de carbone est apolaire au niveau de la géométrie de ces molécules ?
.
.
.
Complément : électronégativité d'un atome
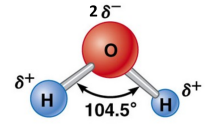
Certains atomes ont une forte électronégativité : ils ont tendance à attirer vers eux les électrons qui constituent la liaison covalente entre deux atomes. Ils portent alors des charges partielles négatives notées \(\delta\).
C'est le cas des atomes d'oxygène et d'azote par exemple.
La molécule d'ammoniac, polaire ou apolaire ?
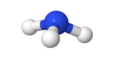
Qu'en pensez-vous ? Justifier votre réponse.
.
.
.
Définition : Solubilité d'une espèce chimique dans un solvant
C'est la masse maximale de soluté que l'on peut dissoudre dans un litre de solvant s'appelle la solubilité : lorsque l'on ne peut plus dissoudre de soluté dans un solvant, on obtient une solution saturée.
Elle s'exprime généralement en g / L.
Remarques :
la solubilité dépend de la température, généralement, elle augmente avec la température.
un solvant polaire dissout uniquement les solutés polaires alors qu'un solvant apolaire dissout uniquement les composés apolaires.
.
Méthode : liaisons hydrogène
Un solvant polaire peut dissoudre un soluté polaire car ils se forment alors des liaisons « hydrogène » .
Expliquer la formation des liaisons hydrogène qui existent entre 2 molécules d'eau à partir du schéma ci-contre.
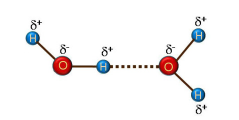
.
.
.